Il Servizio Assistenza Territoriale della Regione Emilia Romagna informa che nell’ambito della procedura di acquisto regionale dei medicinali biologici e biosimilari per gli anni 2020-2024, per quanto attiene all’insulina LISPRO e GLARGINE da DNA ricombinante, sono stati aggiudicati nel mese di novembre 2020 i seguenti prodotti:
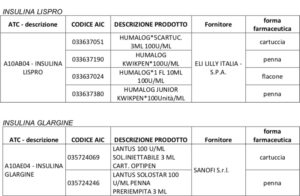
Tali prodotti sostituiscono quelli disponibili dalle precedenti aggiudicazioni: insulina lispro della ditta Sanofi (Insulin lispro Sanofi®) e insulina glargine della ditta Eli-Lilly (Abasaglar®).
“Come noto – si legge nella comunicazione regionale -, una nuova aggiudicazione di farmaco biologico o biotecnologico comporta l’adeguamento della prescrizione da parte del Medico di Medicina Generale o del Diabetologo alla prima occasione di visita in presenza, al fine di trasferire al paziente adeguate informazioni sull’utilizzo del nuovo prodotto e dei suoi device di somministrazione. Considerato il particolare momento di emergenza pandemica e quindi la difficoltà di effettuare visite in presenza del paziente, è possibile procrastinare l’avvio della terapia con il nuovo prodotto alla prima occasione utile“.
Le occasioni – informa la Regione – in cui potrà essere spiegato al paziente come effettuare in sicurezza la sostituzione del farmaco sono le seguenti:
– durante la visita in presenza presso il Medico di Medicina Generale o il Diabetologo;
– in fase di erogazione del farmaco (Distribuzione Diretta o Distribuzione Per Conto) da parte dei Farmacisti ospedalieri e convenzionati, in accordo con il Medico prescrittore
– durante il contatto con l’Infermiere delle cure intermedie.
Per effettuare tale passaggio in sicurezza ed evitare errori nella somministrazione del farmaco, si suggerisce, sulla base di adeguata prescrizione, di:
1. avviare in via prioritaria la sostituzione delle terapie a base di insulina rapida lispro con quella aggiudicata (Humalog®);
2. procedere alla sostituzione delle terapie a base di insulina basale glargine con il nuovo prodotto (Lantus®) dopo il completamento del passaggio di cui al punto 1;
3. informare il paziente che prima della assunzione del nuovo farmaco è assolutamente necessario esaurire completamente la scorta presso il domicilio del prodotto in uso;
4. riservare al solo Diabetologo la gestione dell’eventuale cambio simultaneo delle terapie nei pazienti che assumono entrambe le insuline (rapida e basale) oggetto della presente nota;
5. riservare al solo diabetologo la gestione dell’eventuale cambio dell’insulina lispro Sanofi in cartucce.
Il Farmacista prima di consegnare il nuovo prodotto dovrà avere cura di:
– verificare che il paziente abbia ricevuto adeguate istruzioni sulle modalità d’uso della nuova penna pre-riempita;
– nel caso in cui ciò non sia avvenuto, istruire adeguatamente il paziente mettendo a disposizione la scheda informativa allegata e altri eventuali ulteriori materiali di supporto;
– ricordare al paziente che prima dell’assunzione del nuovo farmaco occorre terminare completamente la scorta del prodotto fino a quel momento in uso.
In allegato materiale informativo riepilogativo sulla sostituzione del farmaco che si chiede di consegnare al paziente.
 Ordine provinciale Medici ed Odontoiatri di Piacenza Benvenuto nell'Ordine Medici di Piacenza
Ordine provinciale Medici ed Odontoiatri di Piacenza Benvenuto nell'Ordine Medici di Piacenza






